1장 알케인과 기초개념 및 기본적인 명명법
1.1 알케인
알케인이란 수 개의 탄소-탄소 단일 결합에 의하여 형성된 탄소 골격을 이루는 기본적인 화합물을 말합니다. 알케인은 비교적인 반응성이 낮지만, 이중결합을 갖는 화합물과 비교하여 자유로운 회전이 가능하여 기본적인 3차원 구조를 설명하는데 용이하다.
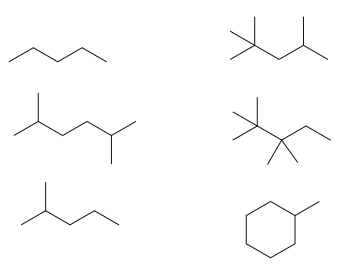
1.2 작용기
화합물을 계열별로 분류가 가능하도록 만들어 주는 구조적인 특징을 작용기라고 합니다. 각각의 화합물들은 구조나 원소의 비율이 달라도, 작용기가 동일하면 유사한 물성을 가지며 유사한 반응에 참여하게 됩니다. 즉, 모든 유기 분자의 화학은 크기나 복잡성에 무관하게 그 분자들이 가진 작용기에 의해 결정됩니다.
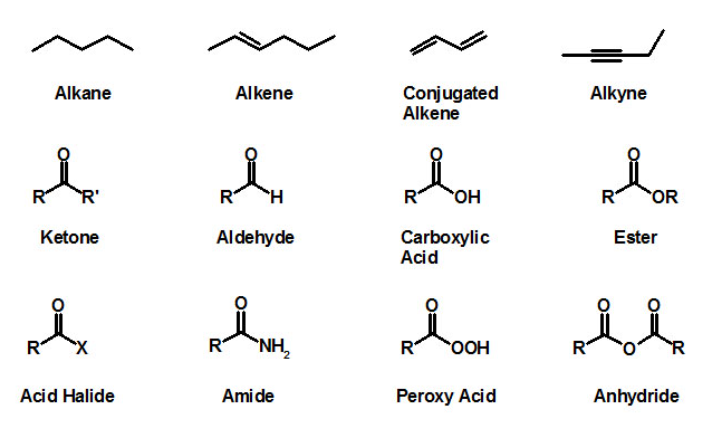
1.3 이성질체
이성질체: 만일 어떠한 화합물이 있는데, 이 화합물과 동일한 분자식을 가지고 있으나 가능한 구조가 두 개 이상일 경우, 그 화합물은 이성질체를 가진다고 합니다.
예를 들어, 아래의 isobutane과 n-butane은 분자식이 C4H10으로 동일하지만, 탄소 골격이 상이하여 이성질체이다.

그리고 이성질체는 다음과 같이 더욱 자세하게 분류할 수 있다.
| 이성질체 | 입체이성질체 | 기하이성질체 |
| 광학이성질체 | ||
| 구조이성질체 | ||
입체 이성질체: 입체 이성질체란 분자식이 동일하고 주사슬과 명명을 통해 배정되는 원소들의 번호는 동일하지만, 배치가 일부 바뀌어 입체적으로 다른 화합물이 가능할 경우 등에서 나타납니다. 입체 이성질체의 예로는 기하 이성질체와 광학이성질체가 있습니다.
→ 기하이성질체: 이중결합으로 연결된 화합물에 있어서, 두 원자 또는 두 치환기의 상대적인 위치로 인하여 다른 화합물을 가질 수 있는 경우, 기하 이성질체를 가진다.

→ 광학이성질체: 만일 한 화합물의 거울상이 그 자신과 동일하지 않을 경우, 그 화합물은 광학이성질체를 가진다.
예를 들어, 아래 그림의 전자는 (R)-2-Butanol이고 거울상으로 후자의 구조를 가진다. 그러나 두 화합물은 포개어지지 않으므로 다른화합물이다. 즉, 후자는 (S)-2-Butanol로서 두 화합물은 분자식이 서로 동일하지만 다른 화합물에 속하며 광학이성질체이다.
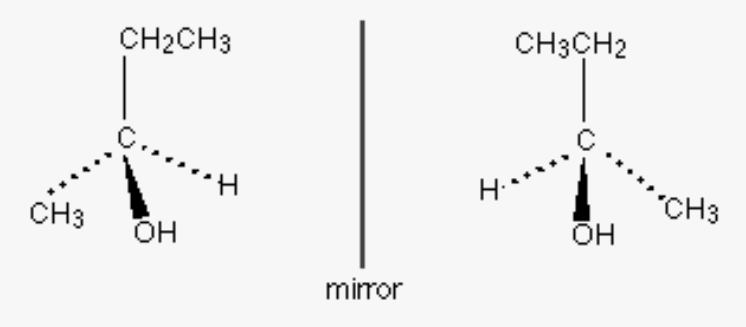
구조이성질체: 구조 이성질체란 분자식이 동일한데도 isobutane과 n-butane의 예시처럼 1) 탄소골격이 다르거나 2) 작용기가 다르거나 3) 선형과 고리 구조 모두 가능한 경우 등에서 나타난다.
2) 작용기가 다른 '구조 이성질체'의 예

3) 선형과 고리구조 모두 가능한 '구조 이성질체'의 예
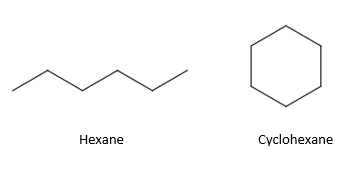
1.4 알킬기
알킬기: 알케인으로부터 수소 원자 하나를 제거한 구조를 알킬기라고 한다. 알킬기는 모체인 알케인의 이름 -ane를 -yl로 바꾸어 명명합니다.
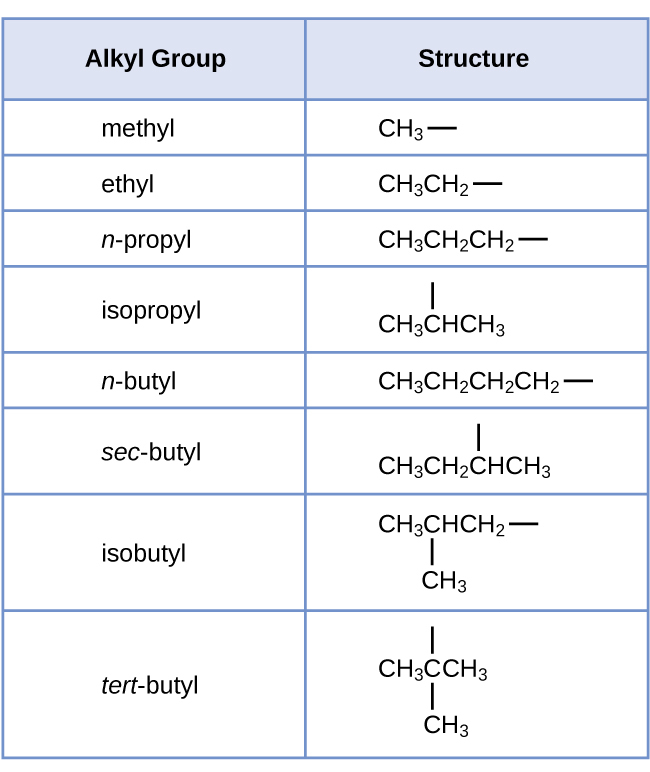
※ sec-, tert- 등은 수소원자가 제거된 탄소의 차수를 말한다. 참고로 차수란 탄소원자가 몇 개의 탄소원자와 결합한 개수와 동일하다. 예컨대, tert-butyl과 같이 중심 탄소가 3개의 탄소와 결합하므로 tert- 접두어를 사용하여 명명한다. (sec-는 2차를 의미)
1.5 알케인의 명명법
대부분의 유기화합물들은 다음의 순서를 통해 명명합니다.
단계 1. 가장 긴 탄소 사슬을 갖는 주사슬을 찾는다.
→ 만일 가장 긴 탄소 사슬이 2개 이상일 경우 곁가지가 많은 사슬을 주사슬로 선택한다.
아래와 같은 경우 탄소를 각각 6개씩 갖는 동일한 길이의 사슬이 있지만, 후자의 경우 곁가지가 2개로 더 많으므로 후자의 빨간선이 주사슬이 됩니다.
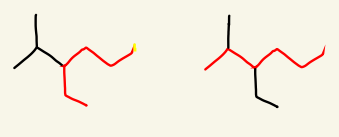
단계 2. 주 사슬에 있는 원자에 번호를 붙인다.
→ 번호는 첫 번째 곁가지에서 더 가까운 쪽부터 시작해서 모체 사슬 각 탄소에 번호를 붙인다.
예를 들어, 아래와 같은 경우 전자와 같이 번호를 매길 경우, 곁가지가 4과 5에 배정되지만, 후자의 경우 곁가지가 3과 4에 배정되어, 후자와 같이 번호를 붙인다.
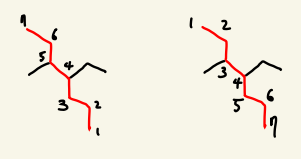
단계 3. 화합물을 '주작용기-접두사-모체-접미사'순서대로 명명한다.
→ 서로 다른 접두사를 쓸 때에는 하이픈을 사용하여 분리하고, 번호를 분리할 경우 쉼표를 사용한다. 만일 둘 이상의 치환기가 존재하면, 알파벳순으로 나열한다. 여기서 주의할 점으로 개수를 의미하는 di-, tri-, tetra-는 고려하지 않는다.
예를 들어, 아래와 같은 화합물은 ethyl과 methyl기가 있으나 e가 m보다 우선하므로 '3-Ethyl-4,7-dimethylnonane'라고 명명합니다.
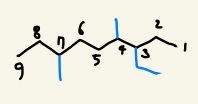
※ 참고로 지금은 간단한 알케인화합물을 다루어 명명이 간단하였으나, 둘 이상의 작용기가 경쟁하여 주작용기를 선정할 필요가 있을 경우, 아래 그림에 표시된 주작용기 순서를 따라서 결정합니다.

'유기화학' 카테고리의 다른 글
| [유기화학] 6장 알켄(Alkene): 반응 및 합성 - 1 (수화 반응, X2 첨가, 옥시 수은 첨가 반응) (0) | 2022.03.11 |
|---|---|
| [유기화학] 5장 알켄(Alkene): 유도효과와 하이퍼콘쥬게이션 및 탄소양이온 자리옮김 (0) | 2022.03.03 |
| [유기화학] 4장 알켄(Alkene): 친전자성 첨가 반응과 마르코프니코프 규칙 (0) | 2022.03.03 |
| [유기화학] 3장 알켄(Alkene)의 불포화도 및 명명법 (0) | 2022.03.01 |
| [유기화학] 2장 사이클로알케인과 입체화학 및 명명법 (0) | 2022.03.01 |




댓글