4장 알켄(Alkene): 친전자성 첨가 반응과 마르코프니코프 규칙
4.1 알켄의 친전자성 첨가 반응
알켄은 파이결합으로 인하여 아래 그림에서 빨간 부분으로 표시된 것과 같이 전자밀도가 매우 높습니다. 이러한 높은 전자밀도로 인하여 알켄은 반응성이 높아져 친전자성 첨가 반응에 참여하게 됩니다.
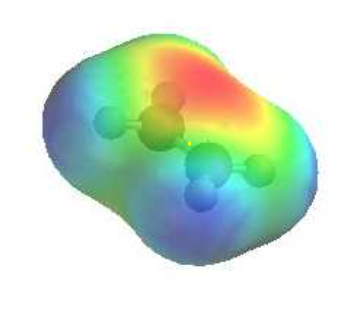
알켄의 친전자성 첨가 반응은 기본적으로 다음 순서의 메커니즘을 통해 일어납니다.
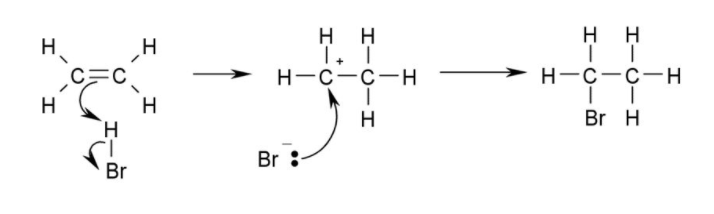
단계 1. HBr에서 전기 음성도가 높은 Br에 의하여 부분적으로 양전하를 띠는 H가 파이전자에 의하여 공격을 받아 새로운 C-H 결합을 형성한다. 이 반응에 의하여 HBr의 결합을 형성하고 있던 2개의 전자가 Br로 이동하여 Br 음이온을 형성한다.
단계 2. Br 음이온이 +전하를 띠고 있는 탄소 원자에 전자쌍을 줌으로써 새로운 C-Br을 형성하고, 전기적으로 중성인 첨가 생성물을 형성한다.
※ 이 때 첨가란 반응 전에 비하여, 반응 후 시그마 결합의 개수가 증가하였음을 의미합니다.
(위의 예시에서는, 반응 전과 비교하여 반응 후에 탄소 원자 간 파이 결합이 끊어지며 시그마 결합이 1개 증가하였습니다. )
· 반응의 의의
이러한 알켄의 친전자성 첨가 반응이 일어나는 이유는, 비록 파이결합을 끊고 시그마 결합을 생성하는 과정에서 에너지가 필요하지만, 반응이 종결된 후 반응 전에 비하여 더욱 안정화된 화합물을 생성할 수 있다는 점에서 의의가 있으며, 이러한 의의가 반응의 추진력으로 작용합니다.
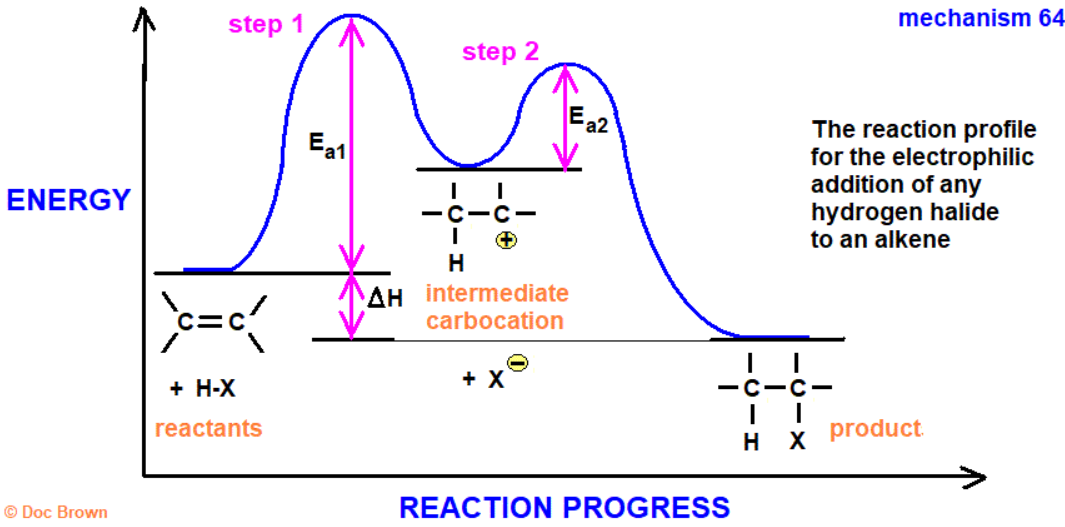
4.2 친전자성 첨가 반응의 방향성: 마르코프니코프 규칙
위치특이성: 알켄의 친전자성 첨가 반응이 일어날 때, 알켄의 치환기가 대칭이 아닐 경우 탄소양이온이 두 가지 방식으로 생길 수 있다. 그러나 실제 반응에서는 일반적으로 한 가지의 탄소 양이온 중간체가 우세하게 형성되며, 하나의 생성물만이 Major 생성물이 되는데, 이처럼 어느 한쪽만의 첨가가 일어나는 반응을 '위치 특이성'이라고 한다.
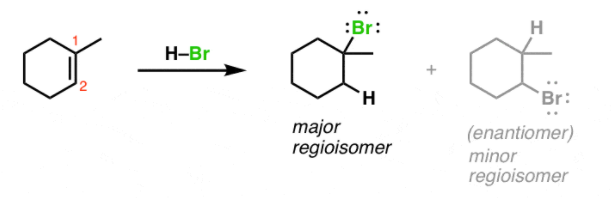
마르코프니코프 규칙: 러시아의 화학자 마르코프니코프가 알켄의 친전자성 첨가 반응에 있어서, 이러한 반응들을 보고 마르코프니코프 규칙을 창시하였다.
→ "마르코프니코프 규칙: 알켄에 HX가 첨가될 때, H는 알킬 치환기 수가 적은 탄소에 결합하고 X는 알킬 치환기 수가 더 많은 탄소에 결합한다."
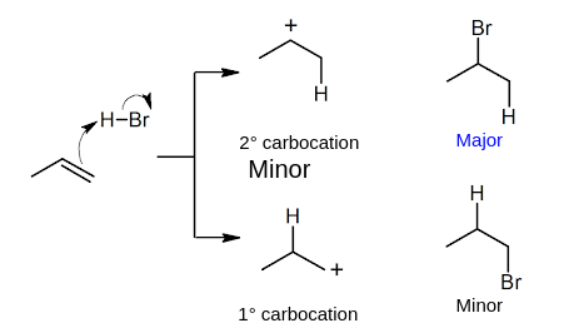
위의 예시에서 반응 시, 상단의 반응을 따르면 2차 탄소 중간체가 생성되며, 하단의 반응을 따를 경우 1차 탄소 중간체가 생성됩니다. 그러나 실제 반응에서는 앞서 언급한 마르코프니코프 규칙을 따라 알킬 치환수가 더 적은 탄소에 H가 결합한 상단의 반응을 거치게 됩니다. 따라서 '2-Bromopropane'이 Major 한 생성물로써 생성됩니다.
'유기화학' 카테고리의 다른 글
| [유기화학] 6장 알켄(Alkene): 반응 및 합성 - 1 (수화 반응, X2 첨가, 옥시 수은 첨가 반응) (0) | 2022.03.11 |
|---|---|
| [유기화학] 5장 알켄(Alkene): 유도효과와 하이퍼콘쥬게이션 및 탄소양이온 자리옮김 (0) | 2022.03.03 |
| [유기화학] 3장 알켄(Alkene)의 불포화도 및 명명법 (0) | 2022.03.01 |
| [유기화학] 2장 사이클로알케인과 입체화학 및 명명법 (0) | 2022.03.01 |
| [유기화학] 1장 알케인과 기초개념 및 기본적인 명명법 (0) | 2022.02.28 |




댓글